过敏原千差万别,但引发的免疫反应却高度一致。花粉、尘螨、真菌等结构迥异的刺激物,均能激活以 IgE 升高和 Th2 反应为特征的二型免疫应答。这一现象长期困扰免疫学界,因传统的“模式识别”理论主要解释一型和三型免疫,强调通过识别保守的病原分子特征触发免疫,而二型免疫缺乏统一的识别机制解释。
2025 年 7 月,北京生命科学研究所/清华大学生物医学交叉研究院徐墨课题组、中科院生物物理所高璞课题组、北生所/清华生物医学交叉研究院邵峰课题组合作,在 Nature 发表重磅研究,题为“Epithelial cell membrane perforation induces allergic airway inflammation”,确定穿孔蛋白 Aeg-S/Aeg-L 是过敏性气道炎症的常见刺激因素之一,可作为普适的二型免疫诱导信号,并揭示了它们的免疫激活机制,填补了该领域长期的空白。

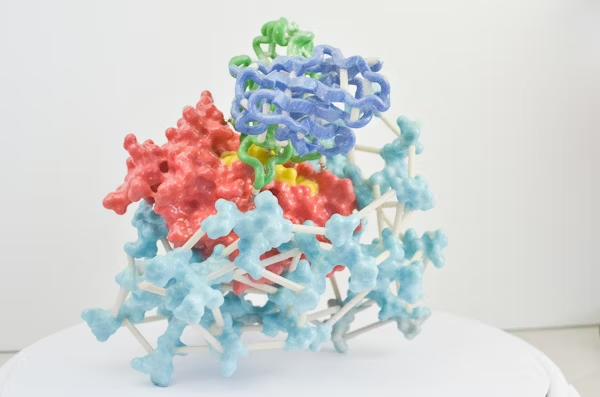
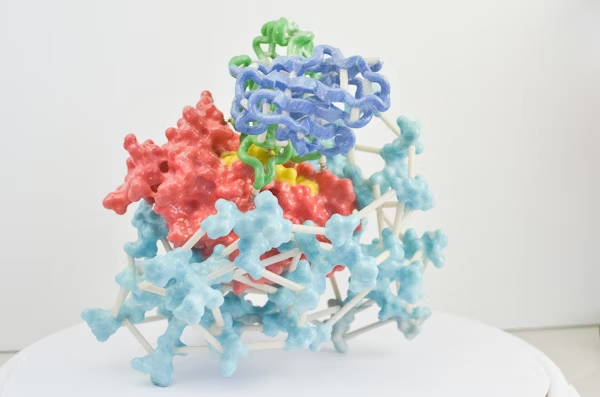
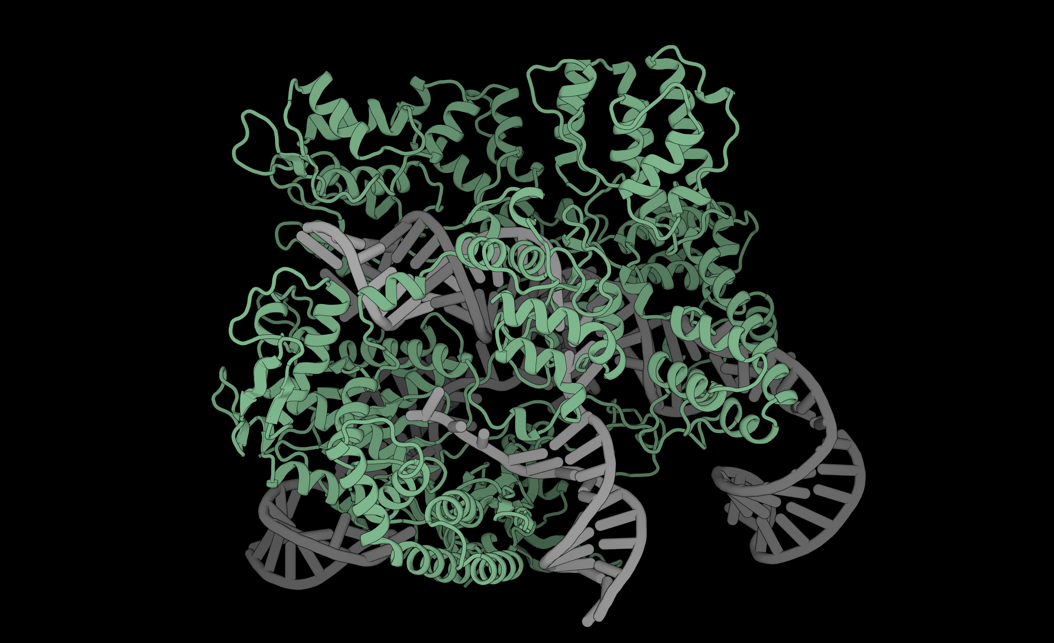
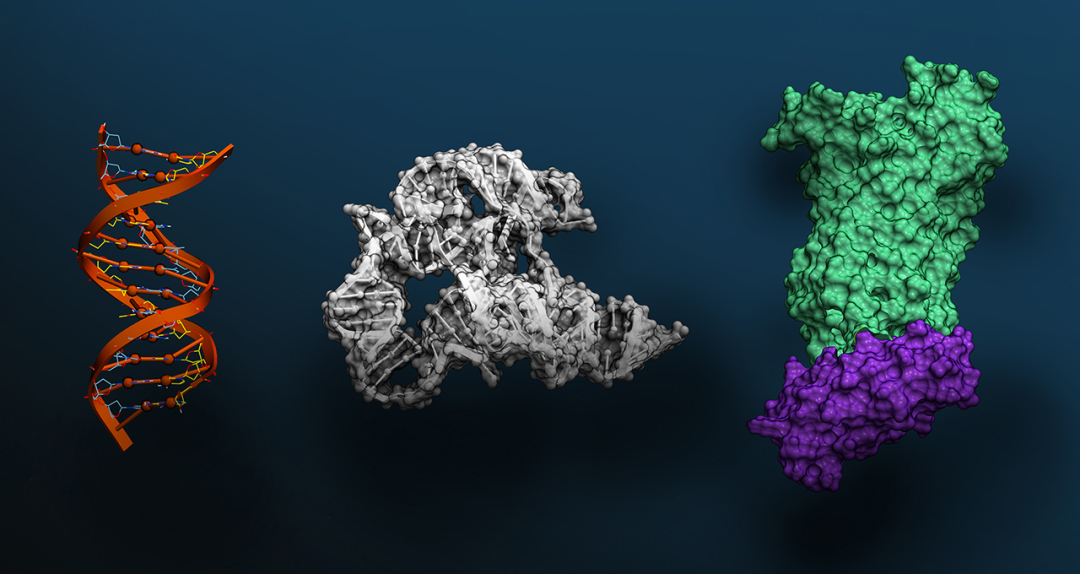
这项研究以广泛致敏的互隔交链孢霉(Alternaria alternata)为研究对象,建立了重构二型免疫早期反应的细胞模型,并在肺上皮细胞中捕捉到 IL-33 释放、MAPK 信号激活以及促炎因子表达三项典型免疫标志。通过六步层析纯化方法,研究团队从互隔交链孢霉中鉴定出协同发挥作用的两种成孔蛋白 Aeg-S 和 Aeg-L,分别属于 aegerolysin 和 MACPF 家族。结构解析显示,这两种蛋白在细胞膜上协同组装为直径约 232 Å 的跨膜孔道复合物,并以 18 聚体形式形成稳定孔道。研究进一步证实,只有 Aeg-S 和 Aeg-L 同时存在,才能构建完整孔道,单独应用任意一种蛋白均不诱导免疫反应。
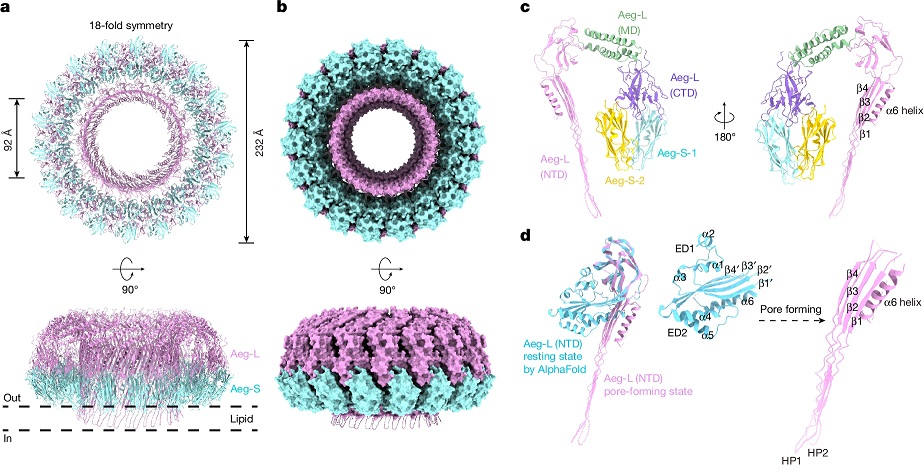
图 | Aeg-S 和 Aeg-L协同组装形成跨膜孔道复合物的冷冻电镜结构
在功能验证中,研究团队将重组 Aeg-S 与 Aeg-L 联合滴鼻给予小鼠,成功诱导出典型的呼吸道过敏反应,包括 IL-33 释放、MAPK 通路激活以及嗜酸性粒细胞浸润、Th2 细胞积聚和 IgE 水平升高。相较之下,单独使用其中任一蛋白不具备诱导能力,而应用基因敲除技术构建的 aeg-s 或 aeg-l 缺失菌株亦完全丧失过敏原活性。回补相应蛋白后致敏能力得以恢复,明确 Aeg-S 和 Aeg-L 是链格孢菌诱导二型免疫的核心活性因子。机制研究显示,孔道形成诱导细胞外钙离子内流,从而激活 MAPK 信号并促进炎症因子表达;同时,细胞损伤释放 IL-33 等警报分子进一步放大免疫级联反应。钙螯合剂或 MEK 抑制剂处理均可阻断信号传导,进一步验证了膜穿孔对免疫激活的直接贡献。
更为关键的是,该机制具有高度普适性。研究团队进一步筛选来自不同物种的七种穿孔蛋白(pore-forming toxins, PFTs),包括真菌来源的 NigA2 和 NigB1、动物来源的 EqtII 和 Lysenin、细菌来源的 PFO、以及其他真菌的 PlyA2、EryB 和 LSL。这些蛋白尽管结构、靶点及孔径均存在显著差异,但当以滴鼻方式反复给予小鼠时,均能诱导呼吸道的典型过敏炎症反应。由此表明,穿孔活性本身即构成二型免疫的通用诱导信号,免疫系统并非依赖分子结构本身识别过敏原,而是响应细胞膜的结构破坏。
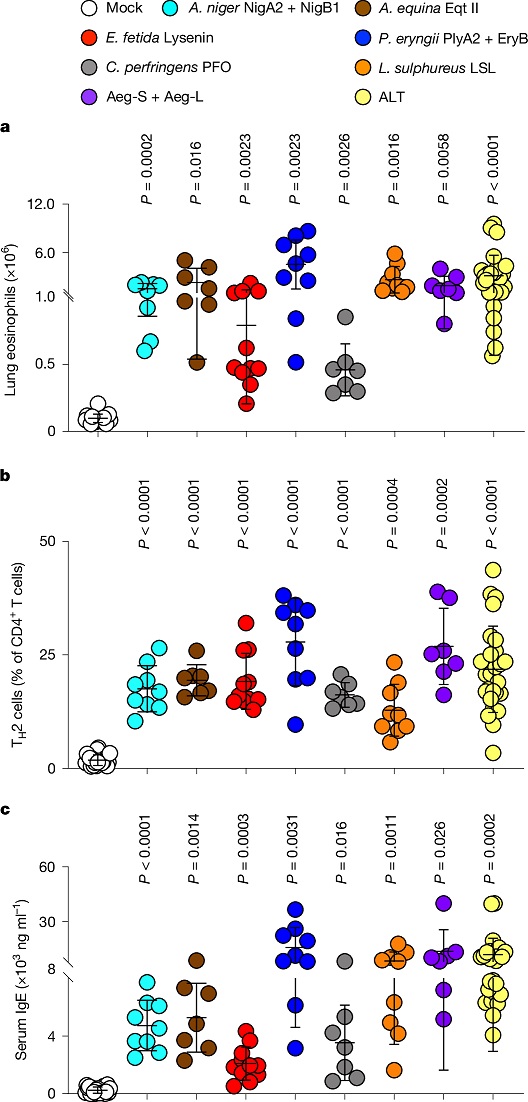
图 | 多种 PFTs 诱发呼吸道过敏
这一发现具有重要理论意义。长期以来,免疫学界将“识别病原分子模式”作为一型与三型免疫的启动依据,而二型免疫由于缺乏一致分子特征的刺激物,其识别机制始终模糊。本研究提出,二型免疫可能并非识别某类分子,而是感知某种组织损伤,特别是上皮屏障结构的扰动。穿孔蛋白诱导的细胞膜破坏,成为启动免疫级联的关键信号。这一机制在霉菌、寄生虫等过敏原中可能具有广泛存在性,打通了对二型免疫识别机制认知的关键环节。
此外,该研究为过敏性疾病的干预提供了新的思路。传统抗过敏治疗多集中于炎症阶段的缓解,而本研究明确了膜穿孔–Ca²⁺ 内流–MAPK 通路–炎症因子表达这一完整轴线,为早期干预提供了可操作的靶点。通过阻断钙信号或 MAPK 通路,实验已证实可以显著抑制炎症因子表达,提示开发以“穿孔–信号”为靶点的小分子药物具有可行性。同时,该研究也为合成生物学提供了新的设计方向。通过改造致敏蛋白的成孔结构域,有望实现低致敏性蛋白的构建,或用于开发标准化的免疫激活工具,以支持二型免疫研究和抗过敏疫苗的开发。
该成果的提出,也引发了进一步的科学问题。例如,膜穿孔在其他组织微环境中是否也能激活相同的免疫反应?组织特异性因子如何调控相同信号的免疫结局?这些问题的回答将依赖于对免疫–屏障–病原三者相互作用的更系统探索。本研究构建的 Aeg-S 与 Aeg-L 诱导系统,将作为关键模型工具持续发挥作用。
这项研究,首次揭示上皮细胞膜穿孔是二型免疫应答的普适性触发机制,填补了免疫识别理论的最后一块拼图。这不仅为过敏性疾病提供了全新的治疗靶点,更为合成生物学改造免疫应答策略奠定了基石。未来,靶向“穿孔-信号”轴的新疗法,有望让亿万过敏患者摆脱困扰。
参考链接:
1.Shi, K., Lv, Y., Zhao, C. et al. Epithelial cell membrane perforation induces allergic airway inflammation. Nature (2025). https://doi.org/10.1038/s41586-025-09331-1
免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。

























































































































































































安各洛(深圳)生物科技有限公司 版权所有