1,6-己二胺(HMD)和 1,6-己二醇(HDO)广泛应用于尼龙、聚氨酯和聚酯等高分子材料的合成。一直以来,它们主要依赖化石原料生产,然而,这种生产方式面临着诸多问题,比如反应条件苛刻、使用有毒原料或中间体、能耗高以及会产生有害副产物污染环境。因此,开发以可再生资源为原料的生物制造路线成为了研究热点。
近期,清华大学陈振、刘德华等人合作利用大肠杆菌作为宿主,通过代谢工程手段构建了一种从葡萄糖直接合成 HMD 和 HDO 的生物催化途径。相关文章以题为“De Novo Production of 1,6-Hexanediol and 1,6-Hexamethylenediamine from Glucose by Metabolic Engineered Escherichia coli”发表在 ACS Synthetic Biology 期刊。

图|从葡萄糖生产 HDO 和 HMD 的工程策略
在该研究中,研究人员巧妙地将整个合成途径拆分为上游的己二酸合成模块和下游的 HMD 与 HDO 合成模块。
在上游的己二酸合成模块中,研究人员选择了逆向 β-氧化途径来合成己二酸,该途径通过一系列酶促反应将乙酰辅酶 A 和琥珀酰辅酶 A 转化为己二酸,涉及多种酶参与。尽管在大肠杆菌和谷氨酸棒杆菌中已成功实现该途径的表达,但由于关键途径酶的活性不足,己二酸的产量受到限制。
为了提高己二酸的产量,研究人员筛选和评估了关键酶 3-羟基己二酰辅酶 A 脱氢酶(paaH)不同来源的催化效率。结果发现,来自粘质沙雷氏菌和解脲沙雷氏菌的 paaH 表现突出,分别产生了 2.64 g/L 和 3.83 g/L 的 3-羟基己二酸。将其它关键酶基因引入菌株发现,优化后的菌株在培养过程中分别积累了 58.17 mg/L 和 65.71 mg/L 的己二酸。解脲沙雷氏菌的 PaaH 在合成己二酸方面优势明显,被选用于后续研究。
在优化己二酸合成模块时,研究人员发现 3-羟基己二酰辅酶A的脱水反应是整个过程的限速步骤,于是对负责该反应的烯酰辅酶 A 水合酶(PaaF)进行优化。一开始,研究人员尝试用其他候选酶替代大肠杆菌的PaaF,但效果不佳。因此,研究人员尝试在大肠杆菌 PaaF 的 N 端融合 SUMO、GST 和 MBP 标签来提高其溶解性,结果显示,带有 SUMO 标签的 PaaF 可使己二酸产量大幅提升。

图|优化 PaaF 后可大幅提升己二酸产量
了进一步提高己二酸产量,研究人员优化了增加代谢前体物质可用性的策略。为了增加琥珀酰辅酶 A 的供应,他们敲除了编码琥珀酰辅酶 A 合成酶 α 亚基的 sucD 基因;为了减少对前体物质乙酰辅酶 A 的竞争,进一步敲除了编码乙酰辅酶 A 乙酰转移酶的 atoB 基因。得到的两种菌株分别产生了 273.49 mg/L 和 362.52 mg/L 的己二酸。
对于下游的 HMD 和 HDO 合成模块,研究人员提出了一种较以往更节能的辅酶 A 依赖途径。此前的合成途径中,己二酸通过羧酸还原酶(CAR)转化为己二酸半醛,随后通过转氨酶(TA)转化为 6-氨基己酸(6-ACA),或通过醇脱氢酶转化为 6-羟基己酸(6-HHA)作为中间体。6-ACA 可以通过包含 CAR 和 TA 的串联反应进一步转化为 HMD,而 6-HHA 可以通过包含 CAR 和 ADH 的串联反应转化为 HDO。此过程消耗 4个 ATP 分子。
新方法中,己二酸首先被转化为己二酰辅酶 A,然后通过乙酰化醛脱氢酶(SucD)还原为己二酸半醛。随后,己二酸半醛可以通过上述相同的下游途径进一步转化为 HMD 或 HDO。与基于 CAR 的两步还原途径相比,辅酶 A 依赖途径仅消耗 2 个 ATP 分子。此外,作为己二酸合成途径中的中间体,己二酰辅酶 A 可以作为后续生物合成模块的直接前体,从而进一步提高整个过程的效率。
两个合成模块构建完成后,研究人员尝试在一株大肠杆菌中构建完整途径,但并未成功。他们推测在单一菌株中表达这一长且复杂的途径可能会对宿主施加显著的代谢负担,从而限制整个转化过程的效率。
为解决这些问题,研究人员还采用了共培养策略,即让上游菌株将葡萄糖转化为己二酸,下游菌株将己二酸转化为 HMD 和 HDO。通过优化共培养体系中两种菌株的接种比例,发现 1:1 的比例可使 HMD 和 HDO 产量最高,分别在 96 h 达到 16.62 mg/L 和 214.93 mg/L 。
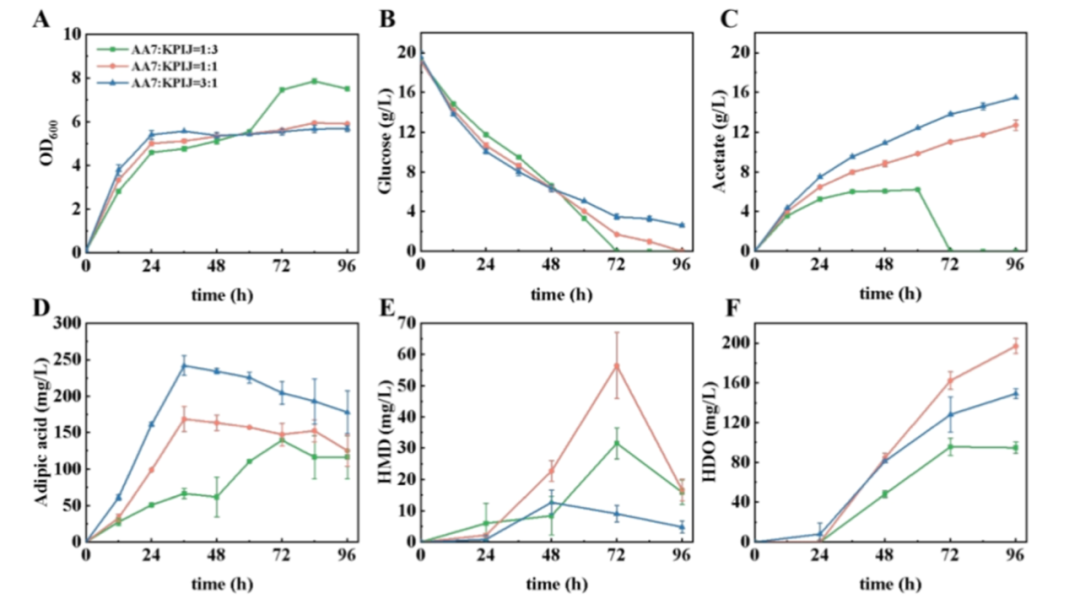
图|共培养体系中,不同接种比例下菌株的生长情况以及 HMD 和 HDO 产量均不同
这些结果成功地证明了使用共培养策略从葡萄糖进行 HMD 和 HDO 从头生物合成的可行性。这种方法实现了代谢途径的物理分隔,减少了代谢负担,并允许独立优化上游和下游模块。但为了实现实际的工业应用,仍需解决若干挑战,包括维持遗传稳定性、确保稳定的种群动态以及实现精确的过程控制等问题,并进一步提高各模块的生产效率。该研究为其他 C6 平台化学品的生产提供了新思路,在未来化工原料生产中具有巨大的潜在价值。
参考文献:
1.https://pubs.acs.org/doi/10.1021/acssynbio.4c00881
免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。
安各洛(深圳)生物科技有限公司 版权所有