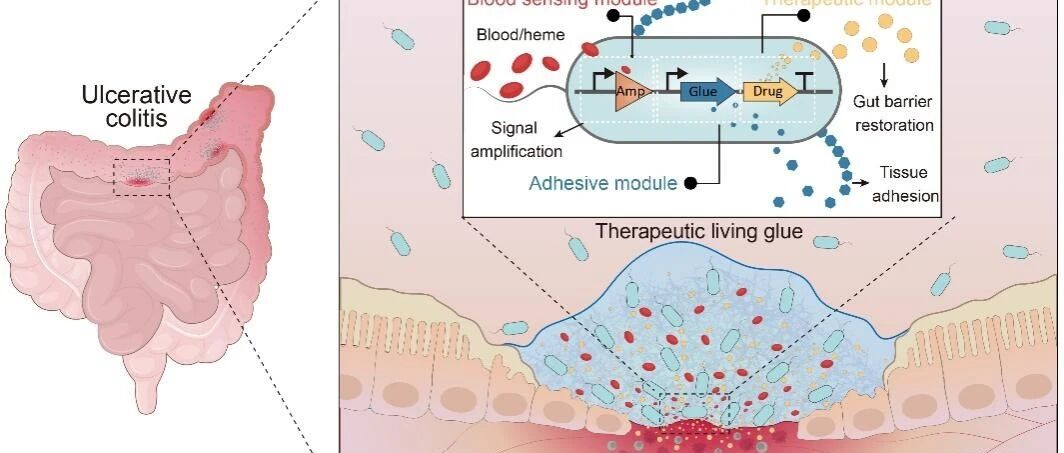
对炎症性肠病(Inflammatory Bowel Disease,IBD)患者而言,反复腹痛、腹泻和便血,往往意味着肠黏膜在破损与修复之间长期拉锯。然而,肠道环境复杂,传统止血剂或黏膜修复药物多为“静态材料”,很难在体内稳定黏附;病灶定位往往依赖影像学或侵入性操作配合。是否有一种治疗材料,能在进入体内后自动识别病灶、黏附,并针对局部持续发挥治疗作用?1月19日,中国科学院深圳先进技术研究院定量合

引言生命的基本单元是细胞,其处理生物分子、生长、传递遗传信息的能力被视作生命的标志。然而,今年早些时候,科学家却发现了一种极其特殊的细胞,其核心功能被削减到了极致,甚至挑战了生物学对“生命”的定义。这是一种仅知其基因序列的单细胞生物,它的基因组小得惊人,仿佛在进化过程中抛弃了绝大部分“家当”。今年五月,研究人员在预印本平台发表了这一发现:该细胞丢失的基因中,包含了参与新陈代谢过程的核心部分。这意味

细菌是生命演化的原初形式也是人类生存环境的重要组成部分细菌为何会演化成超级细菌我们有办法应对超级细菌感染吗央视纪录片频道联合我国多个顶尖实验室推出纪录片《生命如何影响生命》纪录科学家在生命健康领域的突出成就借助生命科学的力量越来越多的疾病有了被治愈的希望本期节目让我们走进中国科学院深圳先进技术研究院听听科研人员怎么说iSynBio造物超级细菌,源于人类自身超级细菌并非天生“超级”,它们是在人类广泛
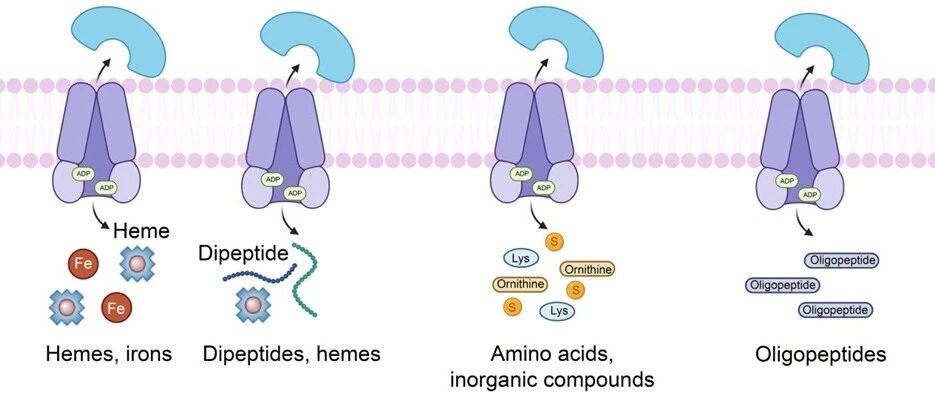
自然界中,几乎所有生命都使用同一套“语言”——由 20 种氨基酸组成的遗传字母表。尽管科学家们后续发现了硒代半胱氨酸和吡咯赖氨酸这两种特殊氨基酸,但天然“字母”的数量依然有限,这从根本上约束了蛋白质结构功能的多样性。为了突破这一天然限制,一种名为“遗传密码子扩展技术”(Genetic Code Expansion, GCE)的工具应运而生。通过引入非天然氨基酸(non-canonical amin
两种简单分子——半胱氨酸和硫酯的反应,或许揭示了生命最初的组成单元是如何被“封装”进细胞膜中。生命的诞生,必然需要一些基本的组成单元。作为遗传物质的DNA和RNA至关重要,它们主导着蛋白质的合成。但还有一类分子,虽然常被常被公众忽视,却同样是生命不可或缺的基石,那就是脂质。地球上几乎所有的生命体都依赖细胞膜。细胞膜由磷脂(属于脂质中的类脂)、蛋白质和糖类等组成,不仅将细胞内部与外部环境分隔开,还负

现在的mRNA技术经常被用于疫苗开发,不过万事皆有例外,mRNA的潜力不止于此。最近一组澳大利亚的研究团队认为,或许mRNA转染能从底层设计上改变抗体的生产工艺。这项研究题为《通过mRNA转染在哺乳动物细胞中快速表达治疗性抗体》,不仅验证了mRNA作为生物制药生产平台的可行性,还展示了其相较于传统方法的具体优劣。传统方法目前大多数抗体药物都是在中国仓鼠卵巢细胞(CHO细胞)中生产的。这类哺乳动物细

新观点——PD-1 阻断并非单纯 “解除免疫抑制、增强抗肿瘤效应”,还可通过破坏 TDLN(tumour-draining lymph nodes) 中高亲和力干细胞样 CD8+T祖细胞(Stem-like progenitor CD8+T,TSL,核心亚型为 TCF-1+PD-1+SLAMF6high)的维持机制,呈现 “短期获益与长期风险” 的矛盾。(Inhibitory

2025年12月1日,Generate:Biomedicines宣布,其AI工程设计的长效抗TSLP抗体GB-0895启动两项三期临床研究SOLAIRIA-1和SOLAIRIA-2,以评估GB-0895治疗严重哮喘的成人和青少年患者。根据新闻稿,这是全球首批推进3期临床阶段的长效抗TSLP抗体。值得注意的是,GB-0895仅用时4年就推进到全球3期——体现了AI制药的强大潜力,包括药物研发的速度、
安各洛(深圳)生物科技有限公司 版权所有